המחקר הראשון מסוגו מצא כי הגוף נכנס ל"מצב חיסכון" בעקבות פעילות גופנית – ואף מצמצם את נפח הכבד והכליות


מחקר
המחקר הראשון מסוגו מצא כי הגוף נכנס ל"מצב חיסכון" בעקבות פעילות גופנית – ואף מצמצם את נפח הכבד והכליות

מחקר בינלאומי חדש בהובלת אוניברסיטת תל אביב מסביר מדוע פעילות גופנית לבדה לא תמיד מובילה לירידה במשקל – גם כאשר שורפים מאות קלוריות בשבוע.
המחקר נערך בהובלת ד"ר צחי כנען במעבדה של פרופ' יפתח גפנר מבית הספר לבריאות הציבור ומכון סילבן אדמס למדעי הספורט באוניברסיטת תל אביב, בשיתוף פרופ׳ אד מלנסון מאוניברסיטת קולרדו, פרופ׳ גל דובנוב-רז, פרופ׳ כרמית לוי, פרופ׳ חן לוקסנבורג וסטודנטים וסטודנטיות מהמעבדות.
במשך 12 שבועות, נחקרים עם עודף משקל ביצעו תוכנית הליכה אירובית, 4–5 פעמים בשבוע, בזמן שהחוקרים מדדו הוצאות אנרגטיות, רמות פעילות, תזונה, ושינויים בהרכב הגוף.
למרות הפעילות הגופנית הסדירה, לא נצפתה ירידה במשקל בקרב הנחקרים – וזאת למרות שריפת מאות קלוריות, שיפור הכושר הגופני, עלייה במסת השריר וירידה בשומן. החוקרים מצאו כי למרות השינויים החיוביים, הגוף "הסתגל" למצב החדש.
בנוסף, החוקרים לא מצאו עלייה משמעותית בצריכת המזון, כך שהיעדר הירידה במשקל אינו נובע מאכילה מוגברת, אלא ממנגנוני פיצוי שמקטינים את הוצאת האנרגיה של הגוף.
"הגוף שלנו מתוחכם מאוד - הוא יודע להתאים את עצמו כדי לשמור על איזון."

הליכה אירובית לא מספיקה לירידה במשקל
פרופ' יפתח גפנר מקשר את התופעה לאבולוציה האנושית: "כאשר לא היה בעבר מזון בטווח הקרוב של השבט, נאלצו הציידים והמלקטות להתרחק באופן משמעותי – דבר שחייב צמצום אנרגטי כדי להצליח לחזור לשבט עם מזון."
הממצאים מראים כי עם הזמן, המשתתפים ביצעו את אותן פעילויות יומיומיות, תוך בזבוז פחות אנרגיה. החוקרים גילו כי גופנו מצמצם את "הוצאות האנרגיה" כדי לאזן את העלייה בפעילות הגופנית, דבר שניכר בירידה של כ-5% בנפח הכבד והכליות, הנחשבים לצרכני אנרגיה מרכזיים.
לדברי ד"ר צחי כנען: "הגוף שלנו מתוחכם מאוד - הוא יודע להתאים את עצמו כדי לשמור על איזון. פעילות גופנית חשובה מאוד לבריאות, אבל כשמדובר בירידה במשקל, היא לא תמיד מספיקה לבדה."
"לפעילות הגופנית יתרונות בריאותיים ייחודיים ומשמעותיים, אך היא לא נועדה להוביל לירידת משקל לבדה."
ירידה של כ-5% בנפח צרכני האנרגיה המרכזיים בגוף - הכבד והכליות
לאלו המסתמכים על פעילות גופנית בלבד על מנת לרדת במשקל, פרופ' גפנר מסביר: "כבר שנים שהמדע מראה שירידת משקל מפעילות גופנית נמוכה מהמצופה, ובמחקר זה, נצפה לראשונה המנגנון של כיווץ האיברים שמסביר תופעה זו." למרות היתרונות המשמעותיים של פעילות גופנית, היא לבדה לא תמיד מספיקה לירידה משמעותית במשקל.
ד"ר כנען מוסיף: "ספורט הוא מרכיב חיוני באורח חיים בריא - הוא משפר כושר, מפחית שומן ומשפר מדדים בריאותיים - אך כדי לראות ירידה משמעותית במשקל, יש צורך לשלב גם תזונה מתאימה."
המחקר החדש מזכיר כי הגוף האנושי אינו מתפקד כמכונת שריפת קלוריות, אלא כמערכת מורכבת שיודעת להסתגל, להתייעל ולשמור על איזון.

מחקר
"מדובר בשינוי תפיסתי של ממש - מעבר מטיפול תומך בלבד, לטיפול שממש מצמצם את היקף הפגיעה"

רוב הפגיעות בחוט השדרה נחשבות כיום לבלתי הפיכות, אך פיתוח חדש מציע דרך לצמצם את הנזק כבר בשעות הראשונות שלאחר הפציעה.
המחקר בהובלת ד״ר אנג'לה רובן מהפקולטה למדעי הרפואה והבריאות ע"ש גריי באוניברסיטת תל אביב – יחד עם ד״ר יונה גולדשמיט וסטודנטים יוסף לוין, רוזמרי לבנדר, אלקסנדר יקובצ׳וק, יבגני בניאס ורות בלטובסקי – הצליח להפחית משמעותית את הנזק שנגרם לתאי העצב של בעלי חיים פצועים, ואף לשפר את יכולת התנועה שלהם.
הגישה הטיפולית החדשנית מתמקדת בחומר גלוטמט (glutamate), אשר מצטבר תוך דקות מרגע הפציעה, וגורם לתגובה דלקתית מקומית והצטלקות. בניגוד לשיטות טיפול בעבר שניסו לחסום את הפעילות המזיקה במוח, החוקרים הצליחו להוציא את עודפי הגלוטמט דרך מחזור הדם בשעות הראשונות לאחר הפגיעה.
על ידי הפחתת רמות הגלוטמט, הצליח צוות המחקר למנוע הידרדרות בתאי עצב, לשמור על מבנה הרקמה העצבית, ולשפר את יכולות ההליכה והתנועה של בעלי החיים שטופלו כבר ביומיים הראשונים. בנוסף, התפקוד המוטורי של אותם בעלי חיים שקיבלו את הטיפול שופר עד לכ-80% מהתפקוד התקין, בהשוואה ל-20% בקבוצה הלא מטופלת.
החוקרים מצאו כי ניתן להעניק את הטיפול עד כשמונה שעות מרגע הפגיעה - ממצא שהופך אותו ליעיל ומציאותי במצבי חירום. הטיפול, אשר ניתן דרך זריקה לווריד, עשוי בעתיד להיות מותאם לשימוש על ידי צוותי עזרה ראשונה שיוכלו לעצור את נזק הפגיעה תוך דקות.
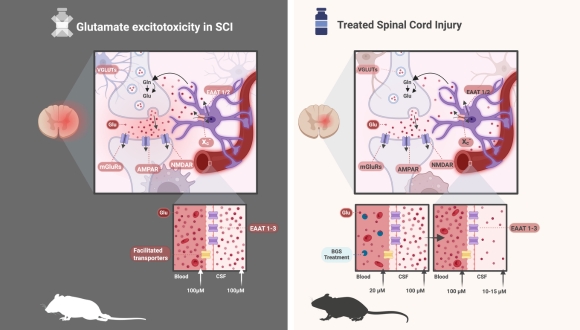
תהליך הטיפול בחוט שדרה של עכברים
לדברי ד"ר רובן, חשיבות המחקר היא ב"עצם היכולת להשפיע על הנזק המשני לאחר הפגיעה, שלב שבו עד כה כמעט ולא היו פתרונות טיפוליים", ובכך "לעצור את 'התגובה השרשרתית' שמובילה להחמרה במצב החולים."
ד"ר גולדשמיט, המתמחה בטיפול ושיקום לאחר פגיעות חוט השדרה ומרצה לפיזיותרפיה בבית הספר למקצועות הבריאות ע"ש שטייר, מוסיפה כי הכיוון הטיפולי החדש עשוי לשנות את אופן הטיפול בשבץ או טראומה מוחית — ולאפשר שיקום מוצלח יותר בהמשך.
בנוסף, במציאות הנוכחית שבה פגיעות ראש כתוצאה מהדף עלו בתדירותן, צוות המחקר החל שיתוף פעולה עם המחלקה לנוירוטכנולוגיה של משרד הביטחון ופרופ׳ חיים פיק, במסגרתו נבחנים טיפולים בבעלי חיים עם פגיעות ראש.
השלב הבא יכלול ניסויים בבני אדם, אותם ד"ר רובן מגדירה כ"פוטנציאל לשינוי אמיתי בגישה הטיפולית לפגיעות חוט השדרה ולמצבים נוירולוגיים נוספים." אם יצליח גם בבני אדם, הטיפול עשוי לשנות את נקודת המוצא של הרפואה - לא רק לנסות לשקם את הנזק, אלא לעצור אותו בזמן.

מחקר
מחקר באוניברסיטת תל אביב חושף שינוי עמוק באופן שבו חומרים משנים מצבי צבירה, באמצעות חלקיקים זעירים שמתפקדים כחיישנים

כיצד נוזל הופך לפתע לחומר קשיח מבלי לשנות את המבנה?
לתעלומה זו, הידועה בשם "מעבר הזכוכית" (glass transition), נמצא פיתרון הודות לפרופ' חיים דימנט ופרופ' יעל רויכמן מביה"ס לכימיה בפקולטה למדעים מדויקים ע"ש ריימונד ובברלי סאקלר, יחד עם קבוצת המחקר של פרופ' סטפן אגלהאף מאוניברסיטת דיסלדורף.
לאחר יותר ממאה שנה של מחקרים, פרופ' דימנט ופרופ' רויכמן סיפקו דרך חדשה להתבונן בתהליך המעבר בין מצבי צבירה, באמצעות מעקב אחר תנועתם של "חיישנים" זעירים בתוך החומר.
צוות המחקר התמקד בחומרים קולואידיים (תערובת של חלקיקים מיקרוסקופיים בנוזל) ומצא שכאשר ריכוז החלקיקים נמוך, המערכת מתנהגת כנוזל רגיל; ככל שהצפיפות עולה, כך החלקיקים מוגבלים בתנועתם, עד שהמערכת כולה "נתקעת" ומקבלת תכונות של מוצק, בדומה לזכוכית.
אותם חלקיקים קטנים וניידים השתלבו בתוך מערכת של חלקיקים גדולים יותר העוברים את המעבר לזכוכית; בעוד שהחלקיקים הגדולים איבדו בהדרגה את יכולת התנועה שלהם, החלקיקים הקטנים המשיכו לנוע – ובכך איפשרו למדוד כיצד משתנה החלל סביבם.

תנועת החלקיקים הקטנים בזכוכיות קולואידליות
החוקרים עקבו אחר זוגות של חלקיקים זעירים בעזרת מיקרוסקופים מתקדמים, ובדקו איך תנועה של אחד מהם משפיעה על השני.
קבוצת המחקר מצאה שכאשר המערכת נוזלית, התנועה "מתפשטת" למרחקים גדולים דרך הנוזל; ככל שהמערכת מתקרבת למצב הזכוכיתי, ההתפשטות נבלמת, והמערכת מתחילה להתנהג כמו חומר מוצק שסופג את התנע במקום להעבירו.
החוקרים זיהו סימנים למעבר בין הנוזל למוצק; לדוגמה, תנועות מנוגדות בין חלקיקים סמוכים, אשר מעידות על היווצרות "התנגדות לגזירה" (shear strength) – כלומר, היכולת של חומר להתנגד לעיוות, אשר אופיינית למוצקים. סימנים אלו אימתו בדיוק רב תחזיות תיאורטיות של אותו הצוות מלפני מספר שנים.
לממצאי המחקר יש השלכות רחבות: השיטה החדשה יכולה לשמש לחקר ג'לים, חומרים רכים, מערכות פעילות ואפילו רקמות ביולוגיות – תחומים שבהם קשה לזהות מתי מערכת מפסיקה "לזרום" ומתחילה להתקשות.
החלקיקים הזעירים בעצם משמשים כ"גששים" מיקרוסקופיים אשר עדים לרגע שבו נוזל מאבד את אופיו, ומאפשרים לבחון את "ההופעה של תכונות מוצקות עוד לפני שהמערכת חדלה לזרום בפועל."
לדברי פרופ' דימנט, "חשיבותו של המחקר אינה רק בזיהוי סימנים חדשים למעבר הזכוכית, אלא בנקודת מבט חדשה על התופעה כולה." ממצאי המחקר "מראים שמעבר הזכוכית אינו מתמצה רק בהאטה הדרגתית של תנועת החלקיקים, אלא מלווה בשינוי עמוק באופן שבו החומר מעביר תנע מנקודה לנקודה."

מחקר
תאורה מלאכותית בלילה עשויה לשבש את המערכת החיסונית של מכרסמי בר, ואף להשפיע על יונקים אחרים

לאחר שמחקרים קודמים הראו כי תאורה מלאכותית משבשת את צרצור הצרצרים, מתברר כעת כי גם יונקים אינם חסינים להשפעותיה.
מחקר חדש מאוניברסיטת תל אביב מצביע לראשונה כי תאורה מלאכותית בלילה – אפילו זו בעוצמה של תאורת רחוב – עשויה לשבש את המערכת החיסונית של מכרסמי בר, ואף להשפיע על יונקים אחרים.
הגר ורדי-נעים, דוקטורנטית בבית הספר החדש לסביבה והפקולטה למדעי החיים ע"ש ג'ורג' ס' וייז, ערכה את המחקר בגן למחקר זואולוגי ע"ש א' סיגלס באוניברסיטת תל אביב, בהנחייתם של פרופ' יריב ויין – ראש המעבדה לאימונולוגיה יישומית בפקולטה למדעי החיים – ופרופ' נגה קרונפלד-שור – ראשת בית הספר לסביבה ורקטורית אוניברסיטת תל אביב.
מטרתה של הגר הייתה לבדוק כיצד תאורה מלאכותית משפיעה על מערכת החיסון של יונקים; הממצאים העידו שאפילו חשיפה מינימלית לתאורה בלילה מגדילה את הסיכון לתמותה פי 2.35.
התגברות על ג'ט לג אחרי טיסה אינה האתגר היחיד לשעון הביולוגי שלנו.
לדברי ורדי-נעים, "חלקים נרחבים בגוף שלנו – ושל כל היונקים – נמצאים תחת רגולציה של שעון ביולוגי", אשר פועל במחזוריות של 24 שעות, "ומותאם למחזור האור והחושך." השעון "משדר לאיברים ולמערכות השונות מה נדרש מהם לעשות בכל שעה", בדומה למערכת החיסון.
חלק מרמות הלימפוציטים בגופנו - תאי דם לבנים המגנים מפני זיהומים, חיידקיים ותאים סרטניים - עולות ויורדות, וכתוצאה מכך, יותר נוגדנים מיוצרים נגד חיידקים או וירוסים בשעות מסוימות.
"הגוף צריך לדעת מה השעה. זיהום האור משנה את המשטר הטבעי של האור והחושך, ומשבש את התאמתו של השעון המרכזי לשעה הסביבתית ומשנה את הדפוסים הללו, כך שלזמן אין עוד הרבה משמעות".
תאי דם לבנים
במחקר כיכבו שני מינים של מכרסמים קטנים החיים במדבר יהודה בנגב: קוצן זהוב, אשר פעיל יותר בשעות היום, ובן דודו הקוצן המצוי, אשר פעיל יותר בלילה.
שני מיני המכרסמים שוכנו ב"תנאי סביבה שמדמים עד כמה שניתן את תנאי הסביבה הטבעיים", כאשר חצי מהמכלאות הוארו בתאורת LED לבנה - "תאורה הנפוצה ביותר היום, ובעוצמה נמוכה יחסית – שמדמה תאורת רחוב." קבוצת הביקורת הושארה בתנאי חושך הנתונים לשינויים בתאורה הטבעית, כמו שמש, ירח וכוכבים.
החוקרים בדקו את אחוז תאי הדם הלבנים בדם המכרסמים במספר נקודות זמן ביממה, וגילו שכמו אצל בני אדם, רמת הלימפוציטים שלהם עולה בשעות המנוחה בין שתיים לארבע בבוקר.
כמות ייצור הנוגדנים בתגובה לאנטיגן (חומר שמערכת החיסון מזהה ומגיבה אליו) הוא תהליך תלוי-זמן; לכן, "חיות שנחשפות לאנטיגן בשעות המנוחה מייצרות הרבה יותר נוגדנים כנגדו מאשר אלו שנחשפו בשעות הפעילות."

הקוצן המצוי
צוות המחקר גילה שהחשיפה לזיהום האור בשעות הלילה טשטשה את דפוסי יצור הנוגדנים בגוף: "במקום מחזוריות של שיא ושפל באחוז הלימפוציטים בדם ובתגובה החיסונית, ראינו השטחה מוחלטת של הדפוסים היומיים." ההשטחה מתייחסת לכך שמערכת החיסון מאבדת את הקשר עם השעון הביולוגי, ובעצם "עלולה להגיב בעוצמה פחות מיטבית לזיהומים ולסטרס סביבתי או לחיסון, מצב שעלול להפוך את בעלי החיים לפגיעים יותר לאורך זמן."
החוקרים משערים כי הפגיעה בתזמון הביולוגי אצל המכרסמים תרמה לירידה בהישרדות, שכן תועדו שיעורי תמותה גבוהים יותר של החיות שהיו חשופות לזיהום אור.
את גורל הקוצנים צוות המחקר רואה כמשל בלבד - וכי "יש להתייחס לזיהום אור כאל גורם סיכון בריאותי סביבתי בעל השלכות רחבות - לא רק על חיות בר אלא גם בהקשר של בריאות האדם והמערכת האקולוגית כולה."
בנוסף, אותם בעלי חיים עם מערכת חיסונית חלשה עלולים להעביר את מחלותיהם לבני אדם, ובכך להשפיע על מערכות החיסון האנושיות; לכן, צוות המחקר "מדגיש את הצורך לבחון מחדש את היקף ועוצמת התאורה הלילית במרחב העירוני והפתוח."
ייתכן שדווקא צמצום התאורה הלילית יסייע להשיב את האיזון הטבעי – ולחזק את חסינותם של יונקים, ובהם גם בני האדם.

מחקר
פריצת דרך במיפוי זרמי האוקיינוס ישירות מהחלל תאפשר העמקה של הבנת שינויי אקלים ויחסי הגומלין בין הים לאטמוספירה

מחקר חדש בהובלת אוניברסיטת תל אביב מציג פריצת דרך בחקר האוקיינוסים: מערכת חדשנית בשם GOFLOW מאפשרת לראשונה למפות תנועות זרימה באוקיינוס ברזולוציה גבוהה במיוחד, ישירות מתמונות לוויין. החוקרים מעריכים כי היכולת החדשה תסייע בהבנה עמוקה יותר של תהליכים המשפיעים על מזג האוויר, על משבר האקלים ועל יחסי הגומלין בין הים לאטמוספירה.
המחקר נערך על ידי פרופסור רועי ברקן, מהחוג לגיאופיזיקה בפקולטה למדעים מדויקים ע"ש ריימונד ובברלי סאקלר, בשיתוף gם לוק לנן ממכון סקריפס לאיקונוגרפיה (Scripps Institution of Oceanography)ֿ, קאושיק סריניבסן מאונבירסיטת קליפורניה לוס אנג׳לס (UCLA) , וניקולס פיזו מאוניברסיטת רוד איילנד (URI). המחקר פורסם בכתב העת Nature Geosciences.
האוקיינוסים מכסים יותר מ־70% משטח כדור הארץ ומהווים מנוע מרכזי בוויסות האקלים הגלובלי. זרמים ימיים, ובהם זרם הגולף שבאוקיינוס האטלנטי, אחראים להעברת חום, פחמן ואנרגיה על פני מרחקים עצומים. אולם עד היום, חלק ניכר מהתהליכים הקטנים והמהירים שמתרחשים בהם – בקני מידה של עשרות קילומטרים ואף פחות – נותרו מחוץ ליכולת המדידה הישירה של לוויינים.
כאן נכנסת לתמונה GOFLOW. המערכת פותחה באמצעות בינה מלאכותית ואומנה על סימולציות אוקייניות מתקדמות במיוחד. היא מנתחת סדרות של תצלומי אינפרה-אדום של טמפרטורת פני הים ומסיקה מהן את שדות הזרימה האופקיים של המים. בניגוד לשיטות קודמות, שהתבססו על הנחות פיזיקליות מגבילות, הכלי החדש מצליח לזהות גם תנועות מורכבות ועדינות יותר.
הניתוח מגלה כי באזורים כמו זרם הגולף מתקיימים תהליכים דינמיים עוצמתיים בקני מידה קטנים מ-30 קילומטרים - תהליכים המלווים בשינויים חדים בטמפרטורה ובהתכנסות זרימה. תופעות אלו קשורות לערבוב אנכי של מים, לעלייה או שקיעה של מסות מים, ולהשפעה על חילופי חום וגזים בין האוקיינוס לאטמוספירה.

פרופ' רועי ברקן
החוקרים מציינים כי למשמעות הממצאים יש היבט אקלימי ברור: תהליכי ערבוב והעברת אנרגיה באוקיינוסים משפיעים על עוצמת סופות, על התפתחות גלי חום ימיים, על פיזור מזהמים ועל יכולת האוקיינוס לקלוט פחמן דו־חמצני מהאטמוספירה. הבנה טובה יותר של מנגנונים אלו עשויה לשפר מודלים לחיזוי אקלים ולספק תחזיות מדויקות יותר לאירועי קיצון.
בנוסף, החוקרים מדגישים כי המערכת מספקת לראשונה ייצוג לווייני ישיר של שדה הדיברגנציה האופקית באוקיינוס - מדד מרכזי להבנת תנועות אנכיות של מים. מדובר במידע שהיה עד כה זמין בעיקר מסימולציות מחשב או ממדידות נקודתיות בים.
פרופסור רועי ברקן מסכם: "האוקיינוס הוא אחד המרכיבים המרכזיים במערכת האקלים של כדור הארץ, אך חלק גדול מהתהליכים שמניעים אותו מתרחש בקני מידה קטנים ומהירים שקשה מאוד למדוד ישירות. באמצעות GOFLOW אנחנו מצליחים, לראשונה, להפיק מהלוויינים מידע דינמי שלא היה נגיש קודם – ולחשוף מנגנונים שמשפיעים על ערבוב, העברת חום וחילופי גזים בין הים לאטמוספירה. בעידן של שינויי אקלים מואצים, היכולת לראות את הפרטים הקטנים הללו היא קריטית להבנה טובה יותר של התמונה הגדולה".
* פרופ' רועי ברקן הוא חוקר בחוג לגיאופיזיקה באוניברסיטת תל אביב, המתמחה באוקיינוגרפיה פיזיקלית ובדינמיקה של נוזלים. מחקריו מתמקדים בהבנת תהליכים דינמיים באוקיינוס בקני מידה קטנים ובינוניים, ובאופן שבו הם משפיעים על ערבוב המים ועל חילופי אנרגיה וגזים בין הים לאטמוספירה. עבודתו משלבת שימוש במודלים נומריים מתקדמים, נתוני לוויין וכלים טכנולוגיים כמו בינה מלאכותית כדי לשפר את הדיוק של מודלים אקלימיים וחיזוי זרמים ימיים.